Előny a társadalom számára
Generikus gyógyszerek
A generikus gyógyszerek:
Előny a társadalom számára
Amikor egyre nagyobb az igény a betegek és az egészségügyi szolgáltatók részéről, a költséghatékony kezelések alkalmazására a generikus gyógyszerek érdemi alternatívát jelentenek. A betegek minőségi, biztonságos és hatékony gyógyszerekhez jutnak elérhető áron, miközben csökkentik az egészségügyi ellátás költségeit is.
A generikus gyógyszerek a „megbízható”, a már több éven át alkalmazott, ún. originális gyógyszerek egyenértékű változatai, ugyanazt a hatóanyagot tartalmazzák,
és „alapvetően hasonlóak” hozzá, ezért felcserélhetőek azzal a terápiás használatban.
A generikus gyógyszerek szigorú ellenőrzésen és értékelésen mennek keresztül mielőtt az európai, vagy a nemzeti hatóságok – ennek megfelelően a magyar hatóság is – engedélyezik a piaci forgalomba kerülésüket.
A generikus gyógyszerek költséghatékonyabbá teszik az egészségügyi rendszer működését és a gyógyszerellátás finanszírozását.
A generikus gyógyszerek:
a megbízható gyógyszerek egyenértékű változatai
A generikus gyógyszerek előállítói saját kutatás és fejlesztés után hozzák ki termékeiket, melyeknek azonos EU-követelményeknek kell megfelelniük, mint az originális készítményeknek.
Egy generikus gyógyszer a Nemzetközi Szabadalmi Jognak megfelelően – a szabadalmi oltalom lejárta után – kerülhet forgalomba. Az adott generikus gyógyszer vagy a nemzetközileg elfogadott, ún. Nemzetközi szabadnéven (INN), vagy a saját márkanevén kerülhet forgalomba. A generikus gyógyszereket széles körben használják számos európai országban a költséghatékony kezelési programok részeként.
A generikus gyógyszerek:
A bioekvivalencia szigorú betartása
A legfontosabb tényező egy generikus gyógyszer előállítása során a bioekvivalencia megállapítása. Bioekvivalencia azt jelenti, hogy amikor tudományosan összehasonlítjuk a generikus gyógyszer és az originális termék hatóanyagának biológiai jelenlétét és hasznosulását (vagyis hogy milyen „ütemben” és mennyiségben van jelen a hatóanyag a szervezetben), akkor azonos dózis alkalmazása esetén azonos eredményt kell kapnunk.
A generikus gyógyszerek:
Hozzájárulás a gazdasági növekedéshez, a munkahely teremtéshez
Az európai generikus gyógyszeripar magasan képzett személyzettel működő fejlett kutatólaboratóriumokat és gyártóhelyeket működtet. Számos európai országban a Medicine for Europe tagvállalatok az egészségügyi rendszerek fő gyógyszeripari szereplői. Ezen felül az európai gyártók a minőségi generikus hatóanyagok vezető exportőrei is, hozzájárulván ezáltal az európai gyógyszeripari kereskedelmi mérleg kedvező alakulásához.
A generikus gyógyszerek:
Elkötelezettség a jövő mellett
A népesség elöregedése és a gyorsan növekvő kezelési költségek arra kényszerítik világszerte a kormányokat, hogy újra és újra felülvizsgálják országaik egészségügyi ellátórendszerének fenntarthatóságát. A gazdaságilag kedvező árú generikus gyógyszerekkel biztosítható, hogy a gyógyszer – ami a leggyorsabban növekvő költségvetési tétel az egészségügyben – költséghatékony felhasználást nyerjen.
Minőség, biztonság, hatékonyság
A generikus gyógyszerek esetében ugyanúgy, mint minden más gyógyszernél (az originális készítményeknél), a tudományosan ellenőrzött minőség mindennél fontosabb. A generikus gyógyszergyártóknak szigorú szabványoknak és előírásoknak kell megfelelniük, ha termékeiket az EU-ban forgalomba kívánják hozni. Az illetékes hatóságokhoz benyújtott dokumentumoknak tartalmaznia kell az alábbiakat:
- a gyógyszer részletes és pontos összetétele (hatóanyagok és segédanyagok);
- a gyártási folyamat leírása
- a gyártási folyamat során alkalmazott ellenőrzési folyamatok leírása
- a hatóanyag és a késztermék gyógyszerészeti vizsgálatainak eredményei;
- a gyártási engedély és a Helyes Gyógyszergyártási Gyakorlat –nak (GMP: Good Manufacturing Practice) való megfelelést igazoló tanúsítvány.
A forgalomba hozatali engedélyezés eljárási rendjei: Nemzeti eljárás; kölcsönös elismerési eljárás (MRP); decentralizált eljárás (DCP); centralizált eljárás; megalapozott felhasználáson (WEU) alapuló engedélyezés.
A forgalomba hozatali engedélyezési eljárás során szakmai hatóság értékeli az új szer minőségét, relatív ártalmatlanságát és hatásosságát. Megfelelés esetén pedig a készítményt államigazgatási határozattal gyógyszerré nyilvánítja.
Bioekvivalencia vizsgálat
Mivel a generikus gyógyszerek ismert, biztonságos és hatékony gyógyszerek, nem szükséges megismételni a preklinikai és a klinikai vizsgálatokat, amelyek szükségesek az originális termék regisztrációjához.
A bioekvivalencia vizsgálatoknak nagy jelentősége van, mert a terápiás egyenértékűséget ez bizonyítja a vizsgált generikus és az originális termék között, az originális terméket használva referenciaként. A generikus gyógyszer és a referencia készítmény bioekvivalensnek minősül (és így helyettesíthető a kezelésben), ha az összehasonlító vizsgálat bebizonyította, hogy a két készítmény esetében nincs jelentős különbség az emberi szervezetben a felszívódási sebesség és eloszlás tekintetében.
GMP: Good Manufacturing Practice
A gyógyszerek gyártása során a szigorú minőségi színvonalat biztosítja.
GMP tanúsítvány szükséges a létesítményekre, személyzetre, eljárási folyamatokra, nyilvántartásra, tárolásra és a szállításra vonatkozóan a követelményeknek való megfelelés igazolására.
„Biostudies”
Bioekvivalencia és biohasznosulási vizsgálatokat tartalmaz, melyben összehasonlítják egy generikus és egy originális gyógyszer hatását, azonos adagolás és azonos feltételek mellett. Ezeket a vizsgálatokat ún. Helyes Klinikai Gyakorlat (GCP: Good Clinical Practice) szabályainak megfelelően kell elvégezni.
Az állatkisérletek és a klinikai vizsgálatok megismétlése szükségtelen és etikátlan
A biostudy azért is fontos, mert megakadályozza, a szükségtelen és etikátlan kísérletek kiterjedt megismétlését embereken és állatokon, miközben továbbra is garantálja, hogy a generikus gyógyszerek ugyanolyan minőségi, biztonsági és hatékonysági előírásnak felelnek meg, mint az innovatív gyógyszerek. A már bizonyított tények megismétlésére vonatkozó vizsgálatok előírása sértené az orvosi kutatás etikai elveiről szóló Helsinki határozatot is.
A generikus minőség: egy jól megalapozott tény
A generikus gyógyszerek gyógyszerészeti minősége és terápiás egyenértékűsége jól ismert ténnyé vált az engedélyezési eljárás során a gyógyszerhatóságok számára, amit a kiterjedt tesztelés, dokumentáció, és ma már gyakran több éves kezelési tapasztalat is bizonyít. A betegek és a politikai döntéshozóknak fenntartással kellene kezelni minden olyan félrevezető információt, amely ennek az ellenkezőjét sugallja. Sőt, azt is tudni kell, hogy az eltérés az originális termék egyes gyártási sorozatai között legalább akkora nagyságrendű, vagy még nagyobb is lehet, mint a statisztikailag kiszámított és szabályozott különbség a generikus gyógyszer és a referencia termék között.
Jogszabályi keretek
Adatkizárólagosság
Az adatkizárólagosság egy olyan intézmény, mely a szabadalmi idő mellett további védelmet képes biztosítani az innovatív gyógyszerek számára azáltal, hogy az adatkizárólagosság időtartama alatt a gyógyszertörzskönyvezés során beadott pre-klinikai és klinikai adatok alapján nem lehet generikus gyógyszereket törzskönyvezni. Az adatkizárólagosság pre-klinikai és klinikai adatok védelmét szolgálja. Új gyógyszer törzskönyvezési kérelmeknél validálási kritérium az adatkizárólagossági nyilatkozat benyújtása. Az adatkizárólagosság időtartama az Európai Unióban egységesen 8 év.
Az adatkizárólagosságon kívül beszélhetünk még az ún. piaci kizárólagosságról, amelynek értelmében az originális gyógyszer törzskönyvezését követően legalább 10 évig terjedő időszak alatt generikus készítményt nem lehet forgalmazni. Amennyiben az adatkizárólagosság és a piaci kizárólagosság egy időpontban kezdődik,
úgy az adatkizárólagosság lejártát követően a generikus gyógyszer regisztrációja és piacra lépésének előkészítése megtörténhet, de a piacra lépéssel meg kell várni a piaci kizárólagosság lejártát is. A piaci kizárólagosság ideje alapesetben 10 év, de ezt meg lehet hosszabbítani további egy évvel néhány esetben.
Az adatkizárólagosság és adatvédelem
Fontos megkülönböztetni az adatkizárólagosságot a kutatási adatok védelmétől, azaz az üzleti titok védelmétől. Az adatkizárólagossági idő lejártát követően, az originális termék dokumentációja még gyakorlatilag korlátlan ideig védettséget élvez a szerzői jogi törvények és egyéb jogszabályok alapján. Tehát, az adatkizárólagosság az innovációt védi, és azt biztosítja az originális gyártó részére, hogy azokat az adatokat, amelyeket ő dolgozott ki és az ő tulajdonában állnak, más gyártó gyógyszer törzskönyvezésére ne használhasson.
Jogi irányelvek
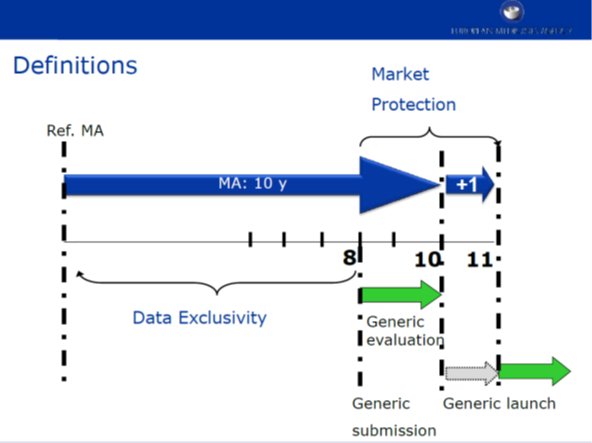
Az Európai Unióban, a közösségi gyógyszerkódex 2005. novemberében hatályba lépett módosítása szerint az „európai referens gyógyszer” első engedélyezésével kezdődően az adatkizárólagosság 8 évig tart, amely mellé 10 év piaci kizárólagosság társul (ha ezek együtt indulnak, akkor a 8 év adatkizárólagosság után további 2 év piaci kizárólagosságról beszélünk). A 10 éves piaci kizárólagosság további maximum egy évvel meghosszabbítható abban az esetben, ha a forgalomba hozatali engedély jogosultja az első 8 év során egy vagy több új terápiás javallatra szerez engedélyt, melyek jelentős klinikai előnnyel rendelkeznek a már meglévő gyógykezelésekkel összehasonlítva. Ez az úgynevezett 8 +2 +1 képlet érvényes az összes tagállamban minden új kémiai entitás-ra (NCE), valamint az előállítási folyamatokra.
A gyakorlatban ez azt jelenti, hogy a generikus gyártó 8 évvel az originális termék megjelenése után már benyújthatja kérelmét a generikus gyógyszer forgalomba hozatalának engedélyezése iránt, de a generikus termék csak 10, illetve 11 év után hozható forgalomba (az eredeti termék megjelenésétől számítva).(Lásd ábra)
Ez azt jelenti, hogy a 2005 novembere után benyújtott generikus gyógyszer kérelmekre vonatkozó 8 +2 +1 éves adatkizárólagossági időszak 2013 végén járt le, azaz előtte nem voltak törzskönyvezhetők. A törvény 1 éves adatkizárólagosságot ad a már használatban lévő gyógyszerek minden új terápiás indikációjára is, amennyiben az megalapozott, de ez csak az új terápiás indikáció igazolásánál érvényes.
A 2019. július 1-jén hatályba lépett hatályba lépett (EU) 2019/933 módosító rendelet bevezette a gyártási jogfeladást a kiegészítő oltalmi tanúsítvány (SPC) által megadott oltalomra a gyógyszerekre vonatkozóan, ami lehetővé teszi az uniós székhelyű vállalatok számára, hogy legyártsák az SPC által oltalom alatt álló gyógyszerek generikus vagy hasonló változatát a tanúsítvány érvényességi ideje alatt, feltéve, ha azt olyan országban kívánják forgalomba hozni, ahol a legyárott termék forgalomba hozatalát szabadalom nem zárja ki, vagy ha a terméket csak a szabadalmi védettség lejártát követően hozzák forgalomba a gyártóhely szerinti országban.
Szellemi tulajdonjogok
A szellemi tulajdon két fő ága az iparjogvédelem és a szerzői jog. Az iparjogvédelmi jogviszony az oltalom megszerzésével jön létre. A szerzői művek esetében a jogviszony a szellemi alkotás létrehozásával keletkezik.
A szellemi tulajdonhoz fűződő jogoknak főbb típusai a védjegy (trademark), formatervezési mintaoltalom (design), a szerzői jog (copyright) és a szabadalmi jog(patent) és a használati mintaoltalom (Utility Model Protection).
- Szabadalmak (Patents)
- Védjegyek (Trademarks)
- Szerzői jogok (Copyright)
- Formatervezési mintaoltalom (design)
- A használati mintaoltalom (Utility Model Protection)
Szabadalmaztatható találmány lehet egy új termék, vagy eljárás, a termék összetétele és annak előállítása, abban az esetben, ha addig ismeretlen termékről/eljárásról van szó, amit a világ egyetlen pontján sem hoztak még nyilvánosságra, és feltalálói tevékenységen alapul. A találmány további előfeltétele, hogy iparilag alkalmazható legyen. Jelenleg külföldi szabadalmi jogszerzést az egyes nemzeti hivataloknál tett bejelentéssel vagy az Európai Szabadalmi Egyezmény (EPC) tagországai esetében ezen túlmenően európai úton is kezdeményezhető. Európai szabadalmi bejelentést az Európai Szabadalmi Hivatalnál (ESZH), illetve a Szellemi Tulajdon Nemzeti Hivatalánál lehet tenni. Az európai szabadalmi bejelentést az ESZH az elsőbbség napjától számított tizennyolc hónap elteltével közzéteszi. Az érdemi vizsgálat kedvező eredmény esetén az ESZH a bejelentésben megjelölt valamennyi ország területére kiterjedő hatályú európai szabadalmat ad a bejelentés tárgyára. A külföldi jogszerzést segíti elő a Szabadalmi Együttműködési Szerződés, melynek keretein belül egyetlen nyelven, egy helyen benyújtott bejelentéssel megindítható a szabadalmi eljárás akár valamennyi szerződő államban. A bejelentés megfelel egy-egy nemzeti (illetőleg regionális) bejelentésnek azokban a szerződő államokban, amelyeket a bejelentő a nemzetközi bejelentésben megjelölt (és amelyek egy regionális szerződés, például az Európai Szabadalmi Egyezmény tagjai). A regisztráció 20 éven át megvédi a feltalálót attól, hogy találmányát bárki másolja, használja, értékesítse, vagy importálja a jogosult engedélye nélkül. A szabadalmi jogok megsértése bírósági eljárást vonhat maga után. Ezen túlmenően a kiegészítő oltalmi rendelet (SPCs), ún. „szabadalmi kiterjesztést”, adhat legfeljebb még 5 évig a gyógyszeripari termékekre, ami 25 évre tolja ki az innovatív gyógyszerek szabadalmi védettségét.
A védjegy vagy „trademark” (logó, szavak, formák, stb.) arra szolgál, hogy egy termék vagy szolgáltatás identitását felismerhetően megkülönböztesse a konkurens termékétől. A védjegy megóvja azokat a jellegzetes komponenseket, amelyek egy termék vagy termék család – beleértve a gyógyszereket is – piaci identitását alkotják. Nemzeti, közösségi vagy nemzetközi szinten veszik nyilvántartásba a védjegyet, amely nemzetközi gyakorlatban lehetővé teszi az ® szimbólum használatát. A védjegyhez fűződő jogok megsértése szintén bírósági eljárást vonhat maga után. A hamisítási esetek felderítésében a vámhatóságok, a rendőrség, vagy a fogyasztóvédelem hivatott közreműködni. A be nem jegyzett védjegy jele nemzetközi gyakorlatban a ™. A védett jelleg feltüntetése a magyar jogszabályok alapján nem kötelező. A fentiek szerint tehát szintén jogi eljárást vonhat maga után, ha egy versenytárs használja a védjeggyel oltalmazott vagy nagymértékben hasonló nevet a termékkel/szolgáltatással azonos áruosztályban.
Az eredeti „kreatív” irodalmi, tudományos és művészeti alkotások védelmére szolgál a szerzői jog, legyen az egy kiadott szöveg, hangfelvétel, film, vagy műsor, függetlenül az adathordozótól. A szerzői jogvédelem alapján a szerzőnek kizárólagos joga van a művének felhasználására, a felhasználás engedélyezésére, azaz egy másolat megvásárlása nem jogosít fel senkit arra, hogy a termékről további másolatokat készíthessen. Korlátozott felhasználás (fénymásolás, szkennelés, letöltés) engedély nélkül is lehetséges, például kutatási célra, e körben ugyanakkor lényeges, hogy a felhasználás jövedelemszerzésre közvetve sem irányulhat. Valakinek a szakmai anyaga vagy idézete csak beleegyezésével jeleníthető meg, viszont egy mű részletét a forrás és a szerző megnevezésével bárki idézheti. Egy ötlet önmagában nem jogvédett csak a megjelenítési formája az. Nincs szerzői jog egy címre, szlogenre vagy kifejezésre, bár ezek is bejegyzett védjegyek lehetnek. Szerzői jog vonatkozik az internet weboldalaira is, számos különböző szerzői jog védi őket, ha a mű példányából másolni vagy nyomtatni kíván valaki egy oldalt,az hivatkozással vagy engedéllyel tehető meg. A szerzői jogok tulajdonosának engedélye nélkül egy anyag nem kerülhet fel egy webhelyre (intranetre sem).
A szerzői jog nem kerül bejegyzésre, a szerzőt ezen joga automatikusan, a mű létrejöttétől, azaz a „kreatív” alkotás megszületésétől kezdve megilleti. Szerzői jog védi az EU-ban a szerző életében és a halálát követő 70 évig az eredeti alkotásokat, ezen védelmi idő elteltét követően elsőként nyilvánosságra hozott művet is védi a szerződi jog, méghozzá 25 évig; illetve szerzői jog védi 50 évig a „broadcast” termékeket (hangfelvételek, sugárzott műsorok, filmek) is. A © jel használata a legtöbb európai országban nem szükséges. A szerzői jogok megsértése bírósági eljárást vonhat maga után.
A formatervezési mintaoltalmat olyan termékek védelmére használják, amelyek egyéni jellegűek, illetve újdonságnak számítanak formájukban vagy mintázatukban. Egy terméknek egy mintaoltalma lehet. A formatervezési mintaoltalomnak újnak kell lennie. A mintaoltalom nem lehetséges, ha az új formát a funkció határozza meg. Mintaoltalom szerezhető országos szinten a Szellemi Tulajdon Nemzeti Hivatalánál történő bejelentés alapján, vagy közösségi szinten, mellyel a tagállamok mindegyikében egyidejűleg, egységesen keletkezik oltalom, illetve lehetőség van nemzetközi bejelentésre is, mely a Hágai Egyezmény értelmében Magyarországon is kezdeményezhető. .Az oltalom a bejelentés napjától számított öt évig tart, amelyet további öt évi időtartamra, legfeljebb négy alkalommal meg lehet meghosszabbítani. A bejelentés napjától számított huszonöt év elteltével azonban az oltalom nem újítható meg.
A használati mintaoltalom a szabadalmazható találmány színvonalát el nem érő új szerkezeti kialakítások védelmére szolgáló oltalmi forma. A mintaoltalom alapján a minta jogosultjának kizárólagos joga van arra, hogy a mintát hasznosítsa, illetve, hogy a hasznosításra másnak engedélyt adjon. Az oltalom ideje 10 év, ezt követően a minta közkinccsé válik. A mintaoltalom tartamára évenként fenntartási díjat kell fizetni. A Szellemi Tulajdon Nemzetei Hivatala az engedélyezési eljárás során csupán vélelmezi a minta újdonságát, valamint azt, hogy a minta feltalálói lépés eredményeképpen jött létre, és amennyiben a bejelentés a jogszabály egyéb előírásainak megfelel, a mintára mintaoltalmat ad. Külföldön csak azokban az országokban, lehet használati minta bejelentést tenni, ahol létezik használati mintaoltalom. A többi országban szabadalmi bejelentést lehet tenni, abban az esetben is, ha Magyarországon használati mintabejelentés van. Ha már van Magyarországon szabadalmi bejelentés, akkor a magyar bejelentési naptól számított 12 hónapon belül célszerű megtenni a külföldi szabadalmi bejelentést (vagy bejelentéseket), ekkor lehet a magyar bejelentés elsőbbségét igényelni, ami azt jelenti, hogy a találmány újdonságának vizsgálatakor nem veszik figyelembe az magyar bejelentési napja óta nyilvánosságra jutott cikkeket, publikációkat, előadásanyagokat, sőt, azóta forgalomba hozott terméket sem. Ha a találmány nyilvánosságra jutott és eltelt a 12 hónap, akkor már nem tehető külföldi bejelentés.
Farmakovigilancia
A farmakovigilancia feladata egy adott gyógyszerkészítmény használatának és hatásának folyamatos monitorozása annak érdekében, hogy időben felismerjék és jelenthessék az előforduló mellékhatásokat (ADR – Adverse Drug Reaction).
Törvényi kötelezettség
Minden európai gyógyszeripari vállalat törvényi kötelezettsége monitorozni egy adott gyógyszer használatát és hatását, valamint észlelni, kiértékelni, megérteni és megelőzni a mellékhatásokat vagy bármilyen, a gyógyszer használatával összefüggő esetleges problémát. Ezt a tudományt, valamint a vele kapcsolatos tevékenységek összességét nevezzük farmakovigilanciának.
Mivel egy generikus gyógyszer csak azután kerülhet forgalomba, hogy az eredeti készítmény már sok éven keresztül elérhető volt a betegek számára, az adott hatóanyag hatásai ekkorra már megfelelő mértékben dokumentáltak, biztonsági profilja pedig kellően megalapozott. Ennek eredményeként ezekkel a már jól ismert hatóanyagokkal kapcsolatosan rendkívül ritkán jelentkeznek váratlan mellékhatások. Ugyanakkor, fontos folyamatosan értékelnünk a haszon/kockázat arányt az adott hatóanyagnál arra vonatkozóan, hogy ez pozitív marad-e a teljes életciklus során. Ebből eredően a gyógyszergyártók és -forgalmazók alapvető tevékenységének részét képezi a gyógyszerek felhasználásának és hatásának állandó jelleggel történő ellenőrzése.
Annak érdekében, hogy a legmagasabb szintű biztonsági elvárásoknak is tartósan megfeleljen, a farmakovigilancia újonnan elfogadott jogi keretei e területen világosan meghatározzák a gyógyszeripari vállalatok szerepét és felelősségi körét.
A vállalatoknak:
• megfelelő gyógyszerbiztonsági rendszert kell működtetniük annak érdekében, hogy felelősséget és kötelezettséget tudjanak vállalni az általuk gyártott és/vagy forgalmazott termékekért;
• biztosítaniuk kell azt, hogy képesek végrehajtani a megfelelő intézkedéseket, amikor és ahol arra szükség van;
• minden olyan információt jelenteniük kell a hatóságok felé, ami befolyásolhatja az adott gyógyszerrel kapcsolatos előny/kockázat egyensúlyt;
• ki kell jelölniük egy olyan felelős személyt, aki az EU-ban a vállalat farmakovigilanciával kapcsolatos teendőit állandó jelleggel és folyamatosan ellátja.
A generikus gyógyszeripari szereplők – az összes érdekelt féllel együttesen – elkötelezettek abban, hogy kivétel nélkül megfeleljenek a fenti elvárásoknak és mindent megtegyenek azért, hogy a betegeknél kizárólag biztonságos és hatékony gyógyszerek kerülhessenek felhasználásra.
GY.I.K.
Gyakori kérdések
Mi is pontosan egy generikus gyógyszer?
A generikus gyógyszer tartalmazza ugyanazt a hatóanyagot, mint az originális gyógyszeripari termék. Mivel ugyanúgy működik az emberi szervezetben ezért felcserélhető az originális termékkel. A generikus gyógyszerek akkor kerülhetnek a piacra, amikor az originális készítmények szabadalma lejárt.
Az EU-ban a generikus gyógyszerek vagy együttesen a gyártó cég neve és Nemzetközi Szabadnév (INN) alapján kerül piacra, vagy saját kitalált márkanév alatt. A generikus gyógyszereket egyre gyakrabban használják a háziorvosok, szakorvosok és kórházak éppúgy, mivel hatékony alternatívák, a magasabb árfekvésű innovatív gyógyszerek helyett.
Van-e különbség a generikus- és az originális gyógyszerek között?
A generikus gyógyszer ugyanazt hatóanyagot tartalmazza, mint az innovatív gyógyszer, és ugyanúgy működik az emberi szervezetben. Egyenértékű generikus gyógyszerek tartalmazhatnak különböző segédanyagokat (például a színezékek, keményítő, cukor, stb) melyek hatással lehetnek a méretre, színre, formára, de ezek egyike sem befolyásolja érdemben a készítmény terápiás hatását vagy viselkedését a szervezetben. Néhány esetben, a hatóanyag a generikus termékekben különbözhet „sóformájában„ és „észterek”-ben az originális termékek hatóanyagától. Az eredeti gyártó is módosíthatja a segédagyagokat (sók, észterek) a termékeiben, ezek nem befolyásolják a gyógyszer terápiás hatékonyságát.
Ki ellenőrzi a generikus gyógyszer minőségét, biztonságosságát és hatékonyságát?
Az EU-ban minden gyógyszert akár innovatív termék akár generikus, engedélyeztetni kell, mielőtt gyártásra kerülne illetve elérhetővé válna a betegek számára, Minden EU-tagállam saját felelős hatósága, illetve az Európai Gyógyszerügynökség (EMA) megvizsgálja és kiértékeli minden egyes piacra kerülő gyógyszer minőségét, biztonságosságát és hatékonyságát.
Ahhoz, hogy a forgalombahozatali engedélyt megkapja, a generikus gyógyszernek „bioekvivalens”-nek kell lennie az innovatív termékkel, azaz ugyanúgy kell „viselkednie” a beteg szervezetében. A generikus gyógyszerek ugyanolyan alapos vizsgálaton esnek át, mint az innovatív gyógyszerek.
A generikus gyógyszer tényleg ugyanolyan jó mint az eredetije?
Igen. A generikus gyógyszernek meg kell felelnie pontosan ugyanazoknak a minőségi, biztonsági és hatékonysági előírásoknak, mint az összes többi gyógyszernek. Csak is „GMP” – azaz Helyes Gyógyszergyártási Gyakorlatnak megfelelő, ellenőrzött üzemekben folyhat a gyártásuk. Továbbá épp úgy, mint az originális termékek esetében, piacra kerülésük után is folyamatosan ellenőrzik őket a gyártók és alkalmanként a hatóság.
A generikus gyógyszerek tényleg kevesebbe kerülnek mint az eredeti termékek?
Igen, és a megtakarítás jelentős. Ezen kívül a konkurens generikus termékek piaci jelenléte versenyhelyzetet teremt, amely a szabadalom lejárta után, – sőt néha még előtte is – árcsökkentésre kényszeríti az originális gyógyszer gyártóját.
Milyen módon járulnak hozzá a generikus gyógyszerek a betegek gyógyulásához, illetve a nemzeti egészségügyi rendszerek fenntarthatóságához?
A generikus termékek használatával a nemzeti egészségügyi rendszerek jelentős pénzösszegeket,
sok milliárd eurót takarítanak meg. Az így megtakarított összegek felhasználhatók egyéb szükséges kezelésekre, szolgáltatásokra, valamint új gyógyszerek kutatására. A generikus verseny egyben fontos ösztönző az innovatív vállalatok számára is, hiszen ezáltal is ösztönzi őket a további új, szabadalmazható (originális) termékek kutatására.
Mikor juthat egy uniós beteg generikus gyógyszerhez?
A generikus termékek akkor válnak elérhetővé a betegek számára, amikor az eredeti termék szabadalmi védettsége lejárt.
Mennyi idő, amíg egy eredeti gyógyszer szabadalma lejár?
Mint minden más iparágban, így a gyógyszeriparban is a szabadalmi szabvány idő az 20 év. Egyedülállóan azonban a gyógyszerek és gyártási technológiájuk esetében ez az idő 5 évvel meghosszabodhat egy úgynevezett „Supplementary Protection Certificate” (Kiegészitő Oltalmi Tanúsítvány) elnyerésével.
Mennyi ideig tart regisztrálni egy generikus gyógyszert az EU-ban?
Egy generikus gyógyszer regisztrálási folyamata rendszerint 1-2 év, de néha hosszabb időt vesz igénybe. Számos EU-tagállamban piaci hozzáférhetőségüket még tovább késleltetik –csakúgy, mint az originális termékek esetében- az ártárgyalások és a támogatási rendszerbe való besorolásuk. A generikus gyógyszerek gyártói is sok időt és pénzt fektetnek termékeik kifejlesztésébe, amelyek nem, csupán ” másolatok” ahogy ezt sokan gondolják. Évek telhetnek el, míg egy generikus termék a döntéshozataltól a piacon való megjelenésig eljut.
Mi az az adatkizárólagosság?
Az adatkizárólagosság egy kiegészítő rendelkezés mely az originális termék szabadalmi oltalmát hivatott támogatni. Ez meghatároz egy időszakot, amely alatt a generikus kérelmező nem kérvényezheti terméke forgalomba hozatali engedélyét az illetékes hatóságoktól. Ebből következően a hatóságok által csak akkor lehet kiértékelni és jóváhagyni a generikus gyógyszereket, ha az adatkizárólagossági határidő lejár, kivéve, ha szokatlan és sokkal drágább eljárásokat alkalmaznak, amelyre csak ritkán van példa.
A generikus gyógyszercégek hozzáférhetnek az originális gyógyszerek adataihoz?
Nem, a generikus cégek nem használhatják az originális termék regisztrációs dokumentációjában lévő adatokat. Tény, hogy mivel az innovatív termékek adatait a kifejlesztő sosem osztja meg mással, így nem is tudnák felhasználni azt. A generikus gyógyszerek előállítói saját kutatás és fejlesztés után hozzák ki termékeiket, melyek azonos EU-követelményeknek kell, hogy megfeleljenek, mint az eredeti termékek. Mivel a generikus gyógyszerek már ismert, biztonságos és hatékony hatóanyagokat tartalmaznak, az originális gyártó által elvégzett pre-klinikai vizsgálatokat és a klinikai vizsgálatokat már nem kell megismételni. Sőt, az etikátlan és nemzetközi egyezmény ellenes lenne. A generikus termék originális termékhez viszonyított hatékonyságát és biztonságosságát az illetékes hatóságok ellenőrzik, csak nekik van hozzáférhetőségük azon adatokhoz melyek szükségesek ehhez.